[Coronavirus] Ces savons qui font la peau au virus
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
Une fois à l’intérieur de notre organisme, le SARS-CoV-2, virus responsable du Covid-19 est difficile à combattre, alors ne le laissons pas entrer ! Nous pouvons nous protéger nous, nos proches et la population en général grâce à un geste simple : le lavage régulier des mains. Comment un geste aussi simple peut-il être efficace contre un virus si virulent ?
Qu’est-ce qu’un virus ?
Un virus est un objet de taille nanométrique, d’environ 100 nanomètres de diamètre. Il est 100 fois plus petit qu’une cellule humaine et 1 million de fois plus petit qu’une balle de tennis. Cette nanoparticule se compose d’une enveloppe virale formée de lipides (c’est-à-dire de gras) et de protéines, encapsulant une macromolécule codant le génome du virus.
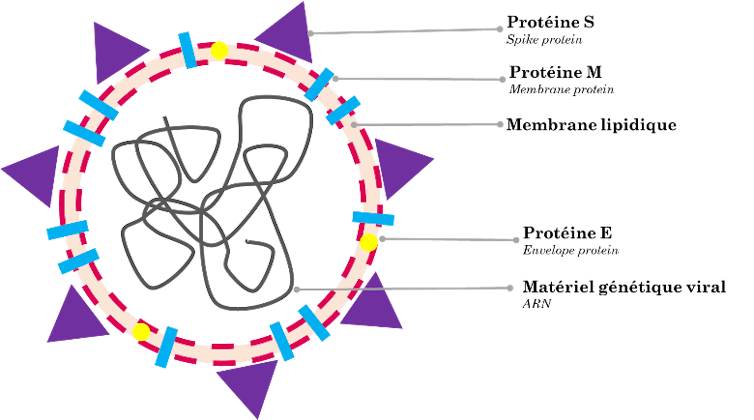
Lise Abiven, Author provided
Comment le savon détruit les virus ?
Nos produits lavants contiennent des tensioactifs. Les tensioactifs sont des molécules pouvant être assimilées à des pieds-de-biche, utilisables à l’échelle nanométrique pour démanteler le virus. Ces molécules sont composées d’une partie qui aime l’eau et d’une autre qui aime les corps gras, on les qualifie d’amphiphiles (« amphi » veut dire « double » en grec). L’enveloppe du virus est un corps gras, comme l’huile par exemple.
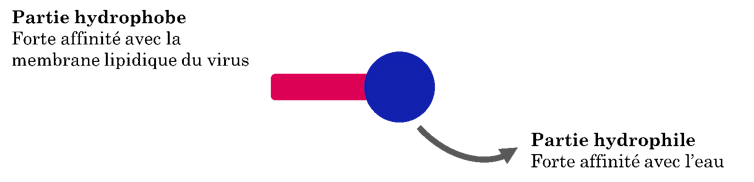
Lise Abiven, Author provided
La partie hydrophobe des tensioactifs contenus dans le savon s’accroche à la membrane du virus et, au moment du rinçage, la partie hydrophile est attirée par les molécules d’eau. La résultante des forces exercées sur le virus entraîne la rupture de son enveloppe lipidique (grasse). Le virus devient inactif et se décroche de la peau grâce à l’action des tensioactifs, du frottement des mains et du débit d’eau.
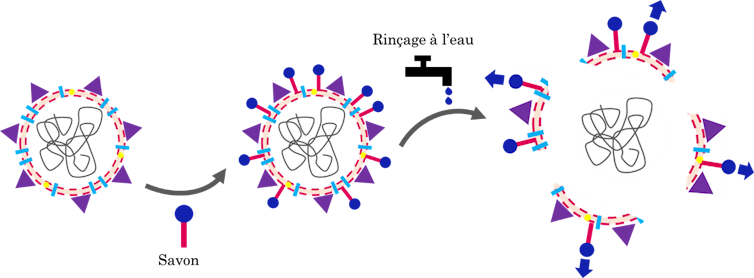
Lise Abiven, Author provided
« Faites l’expérience suivante : Verser un peu d’huile dans l’eau. Les deux corps ne se mélangent pas. Ajouter maintenant du savon et agiter. Que se passe-t-il ? Des microgouttes d’huile se forment dans l’eau sous l’action du savon. On appelle ces particules des micelles. Sous cette forme, l’huile est soluble dans l’eau. »
Pourquoi le virus devient inactif après un lavage des mains avec du savon ?
Un virus n’est pas un organisme autonome : il a besoin d’une cellule hôte pour se reproduire. Le virus y rentre par le même principe qu’une clé dans une serrure. Les protéines S (pour Spike en anglais signifiant pointe), présents au niveau de l’enveloppe virale des coronavirus, se fixent à certains récepteurs cellulaires. Le virus est ensuite internalisé. Une fois à l’intérieur de la cellule, le « virus père » est reproduit par la cellule infectée en plusieurs « virus fils » qui iront à leur tour contaminer les cellules voisines. Le SARS-CoV-2 est un virus à ARN. Cela signifie que son génome est codé sous forme d’ARN, pour acide ribonucléique. L’ARN, tout comme l’ADN, est composé d’une suite de briques chimiques appelés les nucléotides. Par rapport à un virus à ADN, le SARS-CoV-2 gagne du temps ! En effet, l’ARN permet la synthèse directe de protéines, alors que l’ADN doit être d’abord transcrit en ARN avant d’être traduit sous forme de protéines.
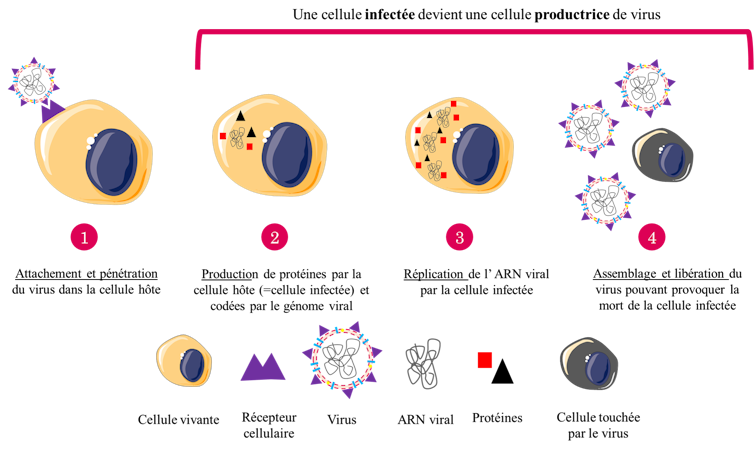
Lise Abiven, Author provided
Lorsque nous lavons nos mains avec du savon, on l’a vu, le savon démantèle l’enveloppe du virus. Ce dernier n’a plus la clé pour entrer dans nos cellules. Le virus est maintenant décomposé en petites parties qui vont se lier aux molécules de tensioactifs du savon pour créer des micelles, solubles dans l’eau. Il se passe le même phénomène que lorsque nous rendons l’huile soluble dans l’eau en ajoutant du savon.
En conclusion, un lavage de mains au savon et à l’eau décompose le virus et le prive de sa capacité à pénétrer dans les cellules, le rendant inactif. Il débarrasse également la peau des fragments de virus comme il le fait pour toutes autres matières grasses (saletés). L’Organisation mondiale de la santé (OMS) recommande de se frotter les mains pendant 20 secondes pour une action efficace sur toute la surface des mains.
Et le gel hydroalcoolique ?
L’alcool en solution dans l’eau (de 60 % à 90 % en volume) dénature certaines protéines de l’enveloppe virale, rendant le virus incapable d’entrer dans une cellule.
Par contre, contrairement au savon qui « lave », le gel hydroalcoolique n’est pas efficace sur des mains sales. L’alcool est désactivé par la présence de matières grasses présentes en trop grande quantité sur la peau (souillures visibles). Le gel hydroalcoolique doit être utilisé sur une peau sèche, non souillées et sans blessures. Ainsi, l’OMS préconise un lavage des mains au savon et à l’eau lorsque nous sommes chez nous et l’utilisation du gel hydroalcoolique lors de nos déplacements pour les courses ou le travail.
Pourquoi le virus s’attache davantage à certaines surfaces plutôt qu’à d’autres ?
Une personne contaminée peut déposer des « gouttelettes » respiratoires, vectrices du virus, sur une surface (plastique, métal, cartons, peau humaine). Une personne non infectée qui touche cette surface peut contracter le virus si elle porte ensuite ses mains à sa bouche, son nez ou ses yeux. Une étude parue dans le The New England Journal of Medicine au début du mois de mars 2020 indique que le SARS-CoV-2 peut être détecté jusqu’à 24 heures sur du carton et trois jours sur du plastique ou de l’acier inoxydable. Même si le virus peut être détecté un certain temps sur une surface, très vite, la charge virale devient trop faible pour nous contaminer efficacement. Au bout de quelques heures, il n’est probablement plus virulent.
L’adhérence des virus aux surfaces se fait principalement via des interactions hydrophobes et électrostatiques. Le virus a une affinité plus ou moins importante avec certains types de matériaux en fonction de ses propriétés physico-chimiques, par exemple la morphologie de son enveloppe, ou sa « charge de surface » qui dicte les interactions électrostatiques. Pour l’instant, le lien entre les propriétés physico-chimiques des virus et la contribution des différentes forces d’interaction n’est pas encore bien établi, mais la physique des principales forces d’interactions en jeu est connue.
Les interactions hydrophobes sont fréquentes dans notre vie quotidienne : si vous déposez une goutte d’eau sur une table, elle n’est pas absorbée par la surface. Le revêtement de la table est hydrophobe et a donc une bonne affinité avec la membrane lipidique du virus.
Pour comprendre les interactions électrostatiques, il faut penser que les contraires s’attirent, et que la matière est constituée d’atomes. Un atome est formé de particules élémentaires chargées positivement – les protons – et négativement – les électrons. De manière générale, la matière est neutre et tend à le rester. Cela signifie qu’elle comporte autant de charges positives que de charges négatives. Les interactions électrostatiques résultent d’un mouvement des électrons d’un corps vers un autre. Elles permettent à la matière de revenir à un état de neutralité lors d’un déséquilibre des charges. La composition chimique de l’enveloppe d’un virus peut lui conférer une charge de surface neutre, positive ou négative.
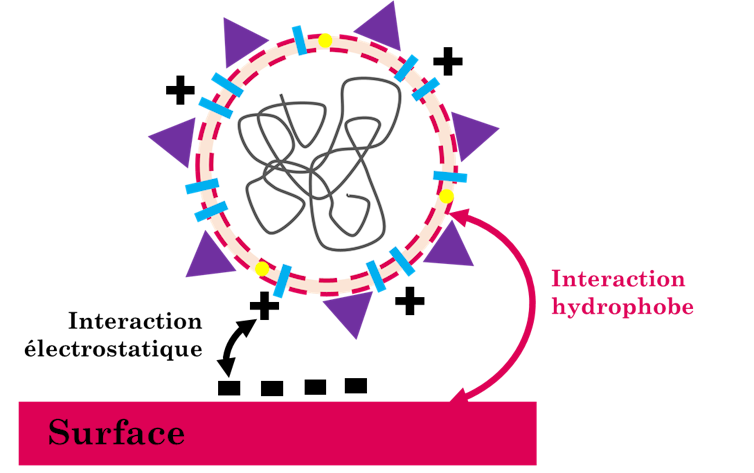
Lise Abiven, Author provided
Si cette charge est négative, le virus va avoir une bonne affinité avec les matériaux ayant une charge positive, c’est-à-dire pouvant présenter un défaut d’électrons en surface comme le papier ou le nylon. Si la charge de surface du virus est positive, ce dernier sera attiré par des matériaux pouvant présenter un excès d’électrons en surface comme certaines matières plastiques telles le PVC ou le film cellophane.
Le développement d’un vaccin contre le Covid-19 est un travail au long cours. Tous ensemble, nous débutons un marathon visant à ralentir sa propagation. En comprenant le virus, sa composition physico-chimique, ses mécanismes d’action et son mode de propagation, nous comprenons aussi les raisons qui rendent les gestes barrières efficaces pour nous protéger et protéger les autres. Mettons-nous dans la peau du virus et nous nous laverons les mains de la bonne manière et au bon moment.![]()
Lise Abiven, Doctorante, Sorbonne Université
