[The conversation] Comment notre corps se défend-il contre les virus ?
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
Marcelo de Carvalho Bittencourt, Professeur – Laboratoire d’Immunologie CHRU de Nancy, Université de Lorraine et Marie Christine Béné, , Université de Nantes
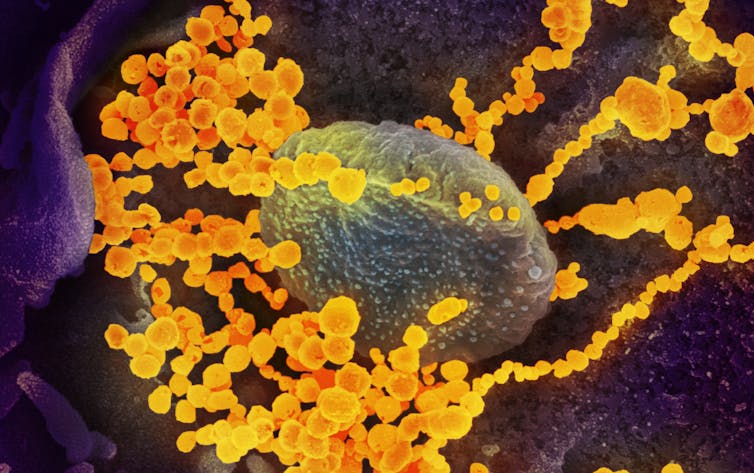
NIAID-RML
En saturant de façon impressionnante les services de réanimation et en se répandant comme une traînée de poudre sur la planète, le coronavirus SARS-CoV-2, à l’origine de la pandémie de Covid-19, a brutalement désorganisé nos sociétés mondialisées.
Médiatisé comme jamais, cet événement a donné lieu à mille avis sur tous les aspects de la pandémie et la manière d’y faire face. Au milieu de ce bruit médiatique, un sujet en particulier mérite notre attention : la façon dont notre système immunitaire fait face au SARS-CoV-2, et aux virus d’une façon générale.
Que se passe-t-il dans notre corps lorsqu’un envahisseur y pénètre ?
D’abord, l’immunité muqueuse
Du bout de notre nez à nos alvéoles pulmonaires et de notre bouche à l’extrémité de notre tube digestif, nos muqueuses sont en contact permanent avec l’environnement. Elles sont parfaitement équipées pour repérer, tolérer ou détruire les éléments qui transitent à leur surface. En effet, la majorité des envahisseurs potentiels (virus, bactéries, champignons, parasites, particules diverses, etc.) pénètre dans l’organisme par le nez, la bouche ou les yeux, et une grande partie d’entre eux finit par arriver dans le tube digestif avant d’être éliminée.
Cette « élimination » utilise les voies naturelles pour tout ce qui n’est pas absorbé par les muqueuses. Ces dernières « trient » les éléments de base des nutriments dont l’organisme a besoin et laissent dans la lumière du tube digestif ce qui n’est pas utilisable. C’est aussi au niveau des muqueuses que débutent les réponses immunitaires qui ciblent les microorganismes.
La première barrière de protection fait intervenir l’« immunité innée ». Celle-ci comprend non seulement des barrières physiques, comme le mucus qui recouvre les muqueuses et empêtre certains envahisseurs (appelés aussi « antigènes », terme désignant tout élément étranger à l’organisme capable de déclencher une réponse immunitaire), mais aussi des cellules capables de détecter rapidement des signaux de danger. Il s’agit essentiellement des cellules dendritiques et des macrophages, qui sont capables d’ingérer les éléments étrangers pour les détruire (cette internalisation est appelée « phagocytose »).
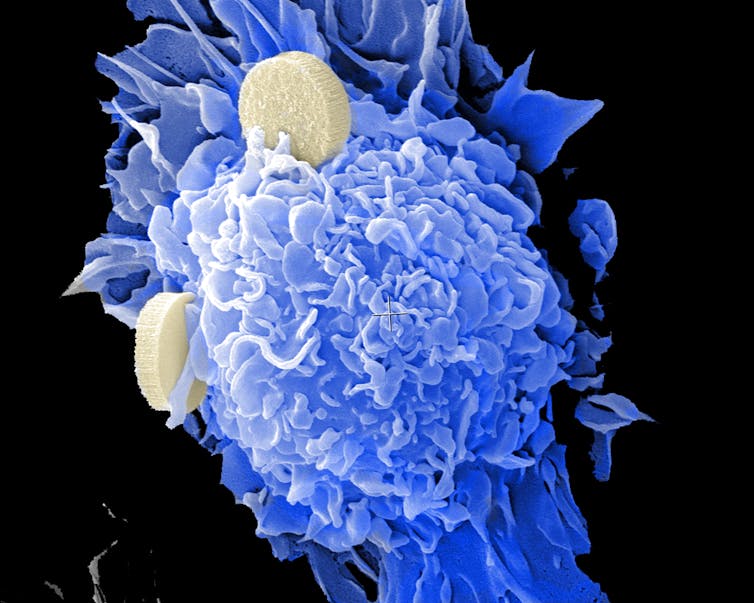
Brenda Melendez, Rita Serda / National Cancer Institute, National Institutes of Health, CC BY
La flore microbienne variée, et globalement bénéfique, qui vit en permanence sur toutes les surfaces de notre corps participe également à l’immunité. Cette flore nous utilise pour l’abriter, mais participe également à la production de certains dérivés de l’alimentation dont nous avons besoin (par exemple la vitamine K, fabriquée par des bactéries présentes dans l’intestin). Elle empêche aussi la prolifération de microorganismes pathogènes, toute en étant tolérée par le système immunitaire.
De nombreux antigènes détectés au niveau des muqueuses sont ainsi rapidement éliminés. Cependant, lorsque cette barrière s’avère insuffisante, l’immunité systémique, parfois appelée immunité « acquise » ou « adaptative », se met en branle. Celle-ci fait intervenir des éléments du système immunitaire qui se trouvent dans le sang : lymphocytes B et lymphocytes T (qui font partie des « globules blancs » spécifiques des vertébrés), immunoglobulines (les célèbres anticorps) et cytokines.
Des sentinelles préparées dès avant la naissance
Il existe deux grands types de lymphocytes, des lymphocytes B, qui produisent les anticorps, et des lymphocytes T, qui interviennent à la fois dans la destruction des cellules infectées, la coordination de la réponse immunitaire et la mémorisation des infections. Tous les lymphocytes prennent naissance dans la moelle osseuse, mais alors que les lymphocytes B y achèvent leur maturation (B pour « bone marrow » en anglais), les lymphocytes T terminent leur maturation dans le thymus (T pour « thymus »).
Outre leur origine, un autre point commun existe entre lymphocytes B et lymphocytes T : tous ont la capacité de reconnaître spécifiquement un, et un seul, motif moléculaire présent à la surface de potentiels envahisseurs. À la surface des lymphocytes se trouve en effet un type de récepteur particulier, le « récepteur pour l’antigène » (appelé BCR pour les lymphocytes B et TCR pour les lymphocytes T). Celui-ci est complémentaire d’un antigène donné : il est capable de s’y attacher, un peu comme deux pièces de puzzle sont capables de s’emboîter ensemble, ou comme un tenon s’associe à une mortaise.
Ce qui est extraordinaire, c’est qu’avant même d’avoir rencontré le moindre envahisseur, l’organisme d’un nouveau-né est déjà capable de reconnaître potentiellement tous les antigènes existants. Dès avant sa naissance, des millions de lymphocytes se sont vus dotés chacun d’un récepteur de l’antigène aléatoire, capable de reconnaître spécifiquement un unique motif moléculaire. En raison du grand nombre de lymphocytes, tous les antigènes existants sont potentiellement détectables : l’organisme a généré un énorme répertoire capable de tout reconnaître, « au cas où » !
Au moment de la naissance, ces millions de jeunes lymphocytes n’ont encore jamais rencontré d’antigène. On les appelle d’ailleurs des lymphocytes « naïfs »… Leur apprentissage immunitaire débute dès les premiers jours de vie, au hasard de ses rencontres avec les antigènes présents dans l’environnement. À cette période, tandis que les premières multiplications de lymphocytes surviennent dans son corps tout neuf, le nouveau-né demeure protégé par les anticorps contenus dans le lait de sa mère, en attendant que les siens puissent prendre le relais efficacement.
Quand un antigène pénètre dans l’organisme, il arrive qu’il atteigne la circulation sanguine ou qu’il entre dans les canaux lymphatiques qui drainent la lymphe (un liquide présent entre les cellules, qui leur apporte des nutriments et évacue les déchets). Dans les deux cas, l’étranger va trouver sur son chemin quantité de lymphocytes B et T stationnés soit dans la rate (organe qui filtre le sang), soit dans les ganglions lymphatiques.
Lorsqu’un lymphocyte « naïf » rencontre son antigène attitré, il commence par se multiplier. Le nombre de lymphocytes capables de reconnaître cet antigène augmente donc lui aussi, ce qui est nécessaire pour s’attaquer aux envahisseurs, qui pénètrent rarement seuls dans l’organisme (et qui s’y multiplient parfois rapidement).
Une partie de ces nouveaux lymphocytes s’attaque aux « intrus » et contribue à les éliminer : ce sont les cellules « effectrices ». Une autre partie reste au repos, prête à se multiplier de nouveau, rapidement lors d’un prochain contact avec le même antigène : ce sont des cellules « mémoire », qui permettent à l’organisme de garder le souvenir de l’infection.
Les lymphocytes B, usines à anticorps
Quand, dans la rate ou les ganglions lymphatiques, un lymphocyte B reconnaît un envahisseur grâce à son récepteur pour l’antigène, le BCR, il commence à se multiplier. Ses innombrables copies se mettent à fabriquer et sécréter des exemplaires solubles de leur BCR : il s’agit des anticorps (ou immunoglobulines). Produits en très grandes quantités, ils se déversent dans les sécrétions des muqueuses ou dans le sang.
Ces immunoglobulines ont la même complémentarité spécifique que le BCR. Elles peuvent donc à leur tour reconnaître l’antigène qui a induit leur sécrétion, où qu’il se trouve, y compris très loin des ganglions lymphatiques ou de la rate. Elles contribuent ainsi efficacement à son élimination. Par ailleurs, à chaque nouvelle stimulation par l’antigène, le taux d’anticorps augmente proportionnellement au nombre de lymphocytes en prolifération, qui ne cesse de croître.
Dans les premiers temps après un contact avec un envahisseur, des immunoglobulines M sont produites. Elles sont moins spécifiques dudit envahisseur que les autres types d’immunoglobulines, et leur concentration diminue rapidement. Mais elles vont alerter le système immunitaire de l’arrivée d’un nouvel « envahisseur » en le piégeant dans un complexe immun (on désigne sous cette expression le résultat d’une interaction entre un anticorps et un antigène).
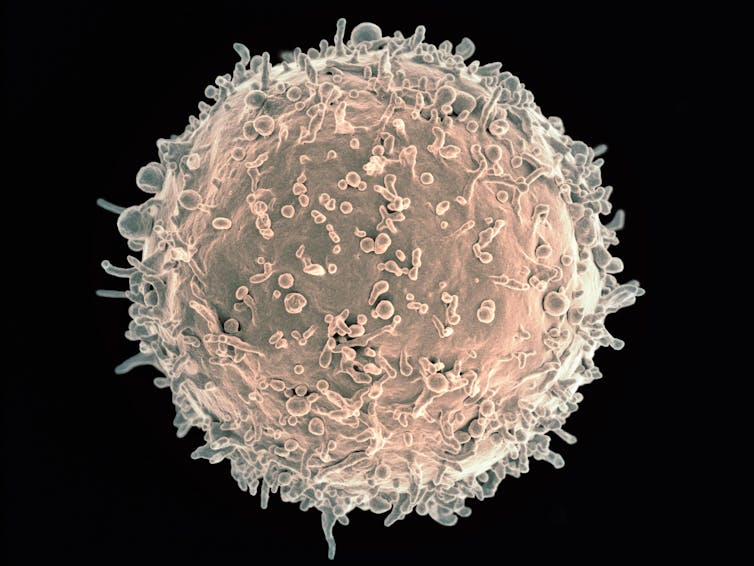
National Institutes of Allergy and Infectious Diseases / National Institutes of Health, CC BY
Le premier niveau de réponse « spécifique », c’est-à-dire l’activation de lymphocytes spécifiques de l’antigène, aboutit à la production d’anticorps particuliers, des immunoglobulines A (IgA), qui sont déversées en quelques heures dans les sécrétions muqueuses par les lymphocytes B qui se sont disséminés dans l’organisme après avoir été activés.
Un peu plus tard seront produites les immunoglobulines G, qui constituent la majeure partie des anticorps présents dans le sang. Elles participent à la lutte contre les envahisseurs, en interagissant notamment avec le système du complément, une composante de la réponse immunitaire innée. Elles sont aussi capables de traverser le placenta, et donc de protéger le fœtus.
Les IgA et les IgG sont capables de se lier aux envahisseurs et de les empêcher d’entrer dans les cellules, notamment dans le cas des virus. On parle alors d’anticorps « neutralisants ». Elles attirent aussi l’attention d’autres cellules du système immunitaire, comme les macrophages, qui vont « manger » les virus emprisonnés par les immunoglobulines par exemple.
La veille des lymphocytes T
Les lymphocytes T possèdent aussi un « récepteur pour l’antigène », le TCR, mais celui-ci diffère du récepteur des lymphocytes B : ce n’est pas une immunoglobuline. Leur TCR permet aux lymphocytes T de reconnaître l’antigène lorsque celui-ci est associé à une des molécules du système HLA (acronyme de « human leukocyte antigen »), qui constituent le « complexe majeur d’histocompatibilité ». Explications : à la surface de toutes les cellules de notre corps, à l’exception des hématies, se trouvent des molécules HLA de classe I (il existe trois classes de protéines HLA). Celles-ci constituent en quelque sorte la « carte d’identité » qui indique aux cellules immunitaires que ces cellules appartiennent bien à l’organisme.
Lorsqu’un virus pénètre dans une cellule, il s’y multiplie. Cette reproduction n’est pas parfaite : elle génère des erreurs, et certaines protéines virales sont mal fabriquées. Elles sont alors découpées en petits morceaux par une petite machinerie cellulaire. Une partie de ces petits morceaux de virus (aussi appelés « épitopes ») s’associe aux molécules HLA de classe I, et l’ensemble remonte à la surface de la cellule.
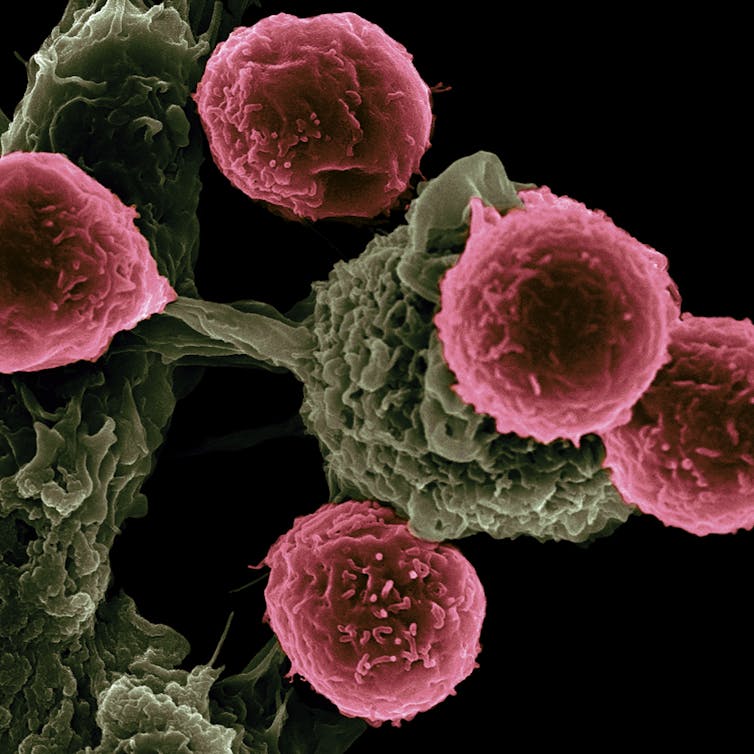
Victor Segura Ibarra, Rita Serda / National Cancer Institute, National Institutes of Health
Si un lymphocyte T passe par là, il va constater que la molécule HLA de classe I a été modifiée (puisqu’elle est maintenant associée à un épitope viral). Tout se passe comme si la cellule lui présentait une carte d’identité falsifiée : le lymphocyte T va alors réagir et détruire cette cellule infectée.
Dans l’espèce humaine comme chez les autres mammifères, le système d’histocompatibilité est extrêmement varié, rendant chaque individu presque unique. Cela signifie que chacun d’entre nous a une façon personnelle de présenter les épitopes viraux à son système immunitaire, certains le faisant de façon plus efficace que d’autres.
Comme les lymphocytes B, dans la rate et les ganglions, les lymphocytes T spécifiques prolifèrent suite à la reconnaissance d’un antigène par leur récepteur de l’antigène. Toutefois, contrairement aux lymphocytes B, ils ne vont pas se contenter de générer une seule catégorie de lymphocytes, mais trois sous populations : des lymphocytes T auxiliaires, des lymphocytes T cytotoxiques et des lymphocytes T régulateurs.
Après avoir été activée par la reconnaissance d’une cellule infectée, chacune de ces sous-populations réagit différemment. Les lymphocytes T auxiliaires sécrètent de nombreuses « cytokines », des messagers chimiques du système immunitaire, qui vont amplifier la réponse des autres lymphocytes, T comme B. Parmi ces cytokines figurent des molécules dont certaines interviennent dans la lutte antivirale et antibactérienne, comme les interférons ou diverses interleukines. Les lymphocytes T cytotoxiques sont quant à eux capables notamment de tuer les cellules infectées par un virus. Enfin, des lymphocytes régulateurs contrôlent les réponses immunitaires en éliminant ou inhibant les lymphocytes T et B effecteurs qui ont joué leur rôle.
Système immunitaire et SARS-CoV-2
Face au SARS-CoV-2, qui est un nouveau virus, nous nous retrouvons tous dans la situation d’un petit enfant. Les lymphocytes naïfs spécifiques d’antigènes portés par ce virus existent au sein de notre organisme. Il faut qu’ils se multiplient pour l’éliminer et générer une mémoire immunitaire, laquelle aura par ailleurs besoin de s’amplifier pour que les réponses soient de plus en plus efficaces.
National Institute of Allergy and Infectious Diseases / NIH
Il est donc théoriquement possible d’être « réinfecté » par le SARS-CoV-2, éventuellement avec des signes cliniques, tant que ce coronavirus persiste dans l’environnement et que notre système immunitaire n’est pas encore assez rapide pour l’éliminer rapidement en cas de nouveau contact. Cependant, les différents mécanismes de la réponse immunitaire systémique sont le plus souvent très efficaces, surtout chez les sujets ayant déjà été immunisés. Ils peuvent alors être totalement silencieux, et l’individu ne se rendra même pas compte qu’il a été en contact avec le virus.
C’est l’objectif de la vaccination : permettre une rencontre avec des motifs viraux ou bactériens en l’absence d’infection, pour entraîner le système immunitaire en prévision de sa rencontre avec le véritable agent pathogène. Lorsque celle-ci surviendra, ses lymphocytes seront prêts à réagir rapidement et efficacement…![]()
